工廠投資構(gòu)成——2016年注冊資產(chǎn)評估師考試《機(jī)電設(shè)備》講義
工廠投資構(gòu)成是資產(chǎn)評估中的重要內(nèi)容之一,特別是在機(jī)電設(shè)備評估領(lǐng)域,對投資構(gòu)成的精準(zhǔn)分析直接關(guān)系到評估結(jié)果的準(zhǔn)確性和可靠性。在注冊資產(chǎn)評估師考試中,對工廠投資構(gòu)成的掌握不僅有助于考生理解機(jī)電設(shè)備的價值形成機(jī)制,還為實(shí)際評估工作提供了理論支持。
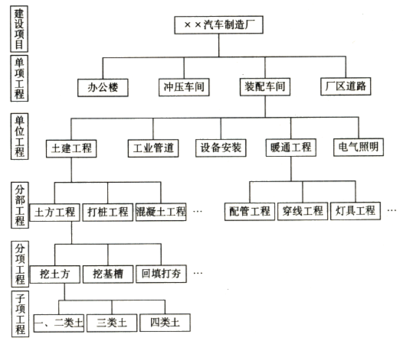
工廠投資構(gòu)成通常包括以下主要組成部分:
- 固定資產(chǎn)投資:這是工廠投資的核心部分,包括廠房、土地、機(jī)械設(shè)備、電氣設(shè)備、運(yùn)輸工具等。在機(jī)電設(shè)備評估中,需重點(diǎn)關(guān)注設(shè)備的原值、使用壽命、折舊情況以及技術(shù)狀況。
- 無形資產(chǎn)投資:包括專利、商標(biāo)、技術(shù)許可等。對于機(jī)電設(shè)備密集型工廠,技術(shù)專利和專有技術(shù)的價值可能占據(jù)重要地位,評估時需結(jié)合市場法和收益法進(jìn)行綜合分析。
- 流動資產(chǎn)投資:如原材料、在產(chǎn)品、產(chǎn)成品及現(xiàn)金等。這部分雖不直接屬于機(jī)電設(shè)備,但會影響工廠整體運(yùn)營效率和價值,評估時應(yīng)考慮其與設(shè)備產(chǎn)能的匹配性。
- 前期費(fèi)用及其他投資:包括工廠籌建期間的設(shè)計費(fèi)、咨詢費(fèi)、培訓(xùn)費(fèi)等。這些費(fèi)用雖不形成實(shí)物資產(chǎn),但作為投資的一部分,需在評估中合理分?jǐn)偂?/li>
在具體評估過程中,注冊資產(chǎn)評估師應(yīng)結(jié)合機(jī)電設(shè)備的特點(diǎn),采用成本法、市場法或收益法進(jìn)行價值估算。同時,注意投資構(gòu)成中各部分的關(guān)聯(lián)性,例如,設(shè)備的先進(jìn)程度可能影響無形資產(chǎn)的價值,而流動資產(chǎn)的充足性則關(guān)系到設(shè)備利用效率。
對工廠投資構(gòu)成的深入理解,有助于提升機(jī)電設(shè)備評估的專業(yè)性和精確度,為考生通過注冊資產(chǎn)評估師考試及后續(xù)執(zhí)業(yè)奠定堅實(shí)基礎(chǔ)。
如若轉(zhuǎn)載,請注明出處:http://www.quadrantepp.cn/product/16.html
更新時間:2026-03-09 14:19:27